2023年9月13日,《自然-通讯》(Nature Communications)在线发表华中科技大学生命科学与技术学院、国家纳米药物工程技术研究中心以及生物无机化学与药物湖北省重点实验室甘璐教授、杨祥良教授团队完成的研究论文“Cell microparticles loaded with tumor antigen and resiquimod reprogram tumor-associated macrophages and promote stem-like CD8+T cells to boost anti-PD-1 therapy”。
肝癌等实体瘤对PD-1抗体治疗应答率相对较低,与肿瘤免疫抑制微环境及肿瘤组织中CD8+T细胞,特别是干性样CD8+T细胞浸润数量不足有关。肿瘤相关巨噬细胞(TAMs)与肝癌的发生发展密切相关,是肝癌免疫微环境的重要组成部分。肿瘤组织中M2型TAMs可通过直接或间接方式抑制CD8+T细胞招募与激活,且因其溶酶体中半胱氨酸蛋白酶高度活化而丧失抗原呈递能力;而M1型TAMs不仅通过吞噬肿瘤细胞清除肿瘤,还可作为抗原提呈细胞向CD8+T细胞呈递肿瘤抗原,启动适应性抗肿瘤免疫,并为干性样CD8+T细胞提供适宜的生存空间。因此,将肿瘤组织中丰富的M2型TAMs重编程为M1型,将有利于改善肿瘤免疫抑制微环境,增加肿瘤组织干性样CD8+T细胞数量,有望改善PD-1抗体肝癌治疗效果。
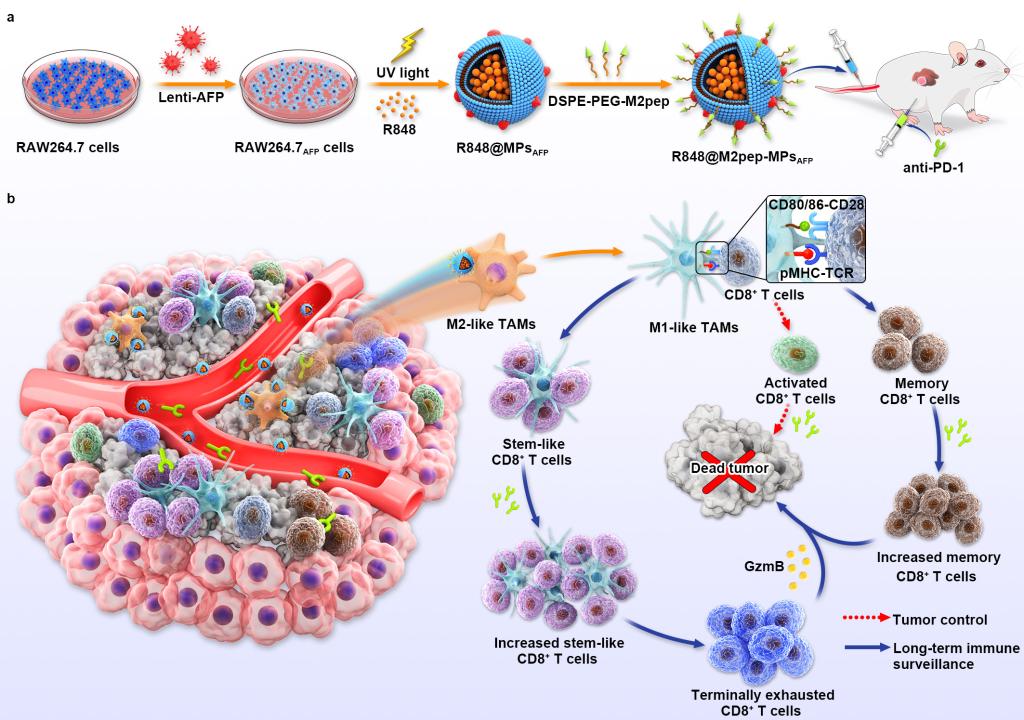
该研究通过对巨噬细胞进行工程化改造,获得过表达肝癌抗原甲胎蛋白(AFP)的微颗粒(MPsAFP),进一步偶联M2型巨噬细胞靶向肽(M2pep),并负载TLR7/8激动剂瑞喹莫德(R848),构建R848@M2pep-MPsAFP纳米药物。利用巨噬细胞来源微颗粒对肿瘤组织的天然靶向性以及M2pep对M2型TAMs的高亲和性,R848@M2pep-MPsAFP靶向递送R848到肝癌组织M2型TAMs,使其逆极化成M1型,改善肝癌免疫抑制微环境,促进CD8+T细胞浸润。另一方面,逆极化后的M1型TAMs将AFP抗原加工后提呈给CD8+T细胞,诱导抗原特异性CD8+T细胞激活;促进干性样CD8+T细胞增殖并分化成具有杀伤效应的终末耗竭型CD8+T细胞。R848@M2pep-MPsAFP与PD-1抗体联用能够产生持久的抗肿瘤免疫记忆,进一步诱导干性样CD8+T细胞增殖分化,显著抑制Hepa1-6皮下、原位肝癌小鼠及二乙基亚硝胺(DEN)诱导的原发肝癌小鼠的生长,有效防止肿瘤复发。此外,利用过表达模式抗原卵清蛋白(OVA)的巨噬细胞来源微颗粒(MPsOVA)制备的R848@M2pep-MPsOVA,可有效改善PD-1抗体对黑色素瘤B16-OVA荷瘤小鼠的治疗效果。该工作提出了一种通用的肿瘤免疫治疗新策略,为发展PD-1抗体等免疫检查点抑制剂赋能技术提供了新思路。
生命学院甘璐教授、杨祥良教授为论文的共同通讯作者,生命学院博士后张晓琼、韦朝晗及讲师雍土莹为论文的共同第一作者。同济医学院附属同济医院张必翔教授、陈孝平院士对该研究给予了大力帮助。该研究得到了国家重点研发计划、国家自然科学基金及博士后科学基金等项目的资助。
甘璐教授、杨祥良教授团队近年来围绕胞外囊泡纳米药物的肿瘤靶向递送、肿瘤微环境改造以及PD-1抗体赋能等开展了系统深入的研究,主要研究成果发表在Nature Biomedical Engineering(2019)、Nature Communications(2019,2021,2022,2023)、Advanced Materials(2022)、Nano Today(2021,2022)、Chemical Engineering Journal(2022,2023)等期刊,部分研究成果正在开展临床转化。
论文连接:https://www.nature.com/articles/s41467-023-41438-9